Robotik KI Chirurgie Trends ist für viele Praxen und Patienten aktuell ein zentrales Thema.
Key-Facts: Die chirurgische Evolution 2026
- Autonomie-Level: Der Übergang von reiner Telemanipulation zu assistierter Teilautonomie (Level 3 Robotics) definiert den Standard im Jahr 2026.
- Daten-Fusion: Die nahtlose Integration von präoperativer Bildgebung (MRT/CT) und intraoperativer Real-Time-Analyse durch KI erhöht die Präzisionsmedizin signifikant.
- Haptik 2.0: Fortgeschrittenes haptisches Feedback ermöglicht Chirurgen, Gewebestrukturen trotz robotergestützter Distanz „zu fühlen“.
- Telechirurgie: Dank flächendeckender 5G-Infrastruktur wird die geografisch entkoppelte Operation zur realen Option für Spezialinterventionen.
- Evidenz: Aktuelle Publikationen in führenden Journals bestätigen die Überlegenheit KI-gestützter Resektionsränder in der Onkologie.
Der Operationssaal der Zukunft ist längst keine abstrakte Vision aus Science-Fiction-Romanen mehr; er ist eine rasch reifende Realität, die sich im Jahr 2026 an einem entscheidenden Wendepunkt befinden wird. Wir stehen als medizinische Gemeinschaft vor einem Paradigmenwechsel, der in seiner Tragweite mit der Einführung der Anästhesie oder der Asepsis im 19. Jahrhundert vergleichbar ist. War die Chirurgie über Jahrtausende hinweg ein rein handwerkliches, auf die manuelle Geschicklichkeit und die visuelle Wahrnehmung des Operateurs beschränktes Feld, so transformiert sie sich nun unwiderruflich in eine datengetriebene Wissenschaft, in der Robotik und Künstliche Intelligenz (KI) als symbiotische Partner des menschlichen Akteurs fungieren. Das Problem, dem wir uns in der konventionellen Chirurgie – und selbst in der klassischen Laparoskopie – gegenübersehen, ist die natürliche Limitation menschlicher Fähigkeiten. Tremor, Ermüdung, eingeschränkte Freiheitsgrade der Handgelenke und vor allem die kognitive Belastung durch die gleichzeitige Verarbeitung komplexer anatomischer Informationen führen zu einer Variabilität in den Operationsergebnissen, die im Jahr 2026 nicht mehr akzeptabel erscheint. Die Diskrepanz zwischen dem, was theoretisch möglich ist, und dem, was im Durchschnitt geleistet wird, muss geschlossen werden.
In der Einleitung dieses Deep Dives müssen wir uns vergegenwärtigen, dass die bloße mechanische Unterstützung durch Roboter, wie sie seit den frühen 2000er Jahren durch Systeme wie da Vinci etabliert wurde, nur der erste Schritt war. Wir bewegen uns weg von der reinen Telemanipulation („Master-Slave-Systeme“) hin zu einer „Digital Surgery“, in der der Roboter nicht mehr nur ein dummes Werkzeug, sondern ein intelligenter Assistent ist. Im Jahr 2026 sehen wir Systeme, die Gewebestrukturen in Echtzeit analysieren, Gefahrenzonen markieren und chirurgische Schritte prädiktiv begleiten. Die Herausforderung für Kliniken, Fachärzte und das Gesundheitssystem besteht darin, diese Technologien nicht nur zu implementieren, sondern ihre tiefgreifenden Auswirkungen auf Ausbildung, Ethik und Patientenpfade zu verstehen. Wie gehen wir damit um, wenn der Algorithmus eine bessere Schnittführung vorschlägt als der Oberarzt? Wie verändern sich Haftungsfragen, wenn teilautonome Systeme eingreifen? Dieser Artikel wird diese Fragen fundiert beleuchten, gestützt auf die neuesten Erkenntnisse der Medizintechnik und evidenzbasierte Daten.
Dabei ist es essenziell zu verstehen, dass es nicht um die Ersetzung des Chirurgen geht, sondern um dessen „Augmentation“ – die Erweiterung seiner sensorischen und motorischen Fähigkeiten. Die Trends für 2026 zeigen eine klare Richtung: Miniaturisierung, Vernetzung und intelligente Assistenz. Wir werden analysieren, wie diese Trias die Patientensicherheit erhöht, die Invasivität weiter senkt und ökonomische Hürden durch neue Marktteilnehmer und modularere Systeme langsam abbaut. Bereiten Sie sich auf eine detaillierte Reise in den hochtechnologisierten OP-Saal des Jahres 2026 vor.
Inhaltsverzeichnis
Grundlagen & Definition: Der neue Standard der Intervention
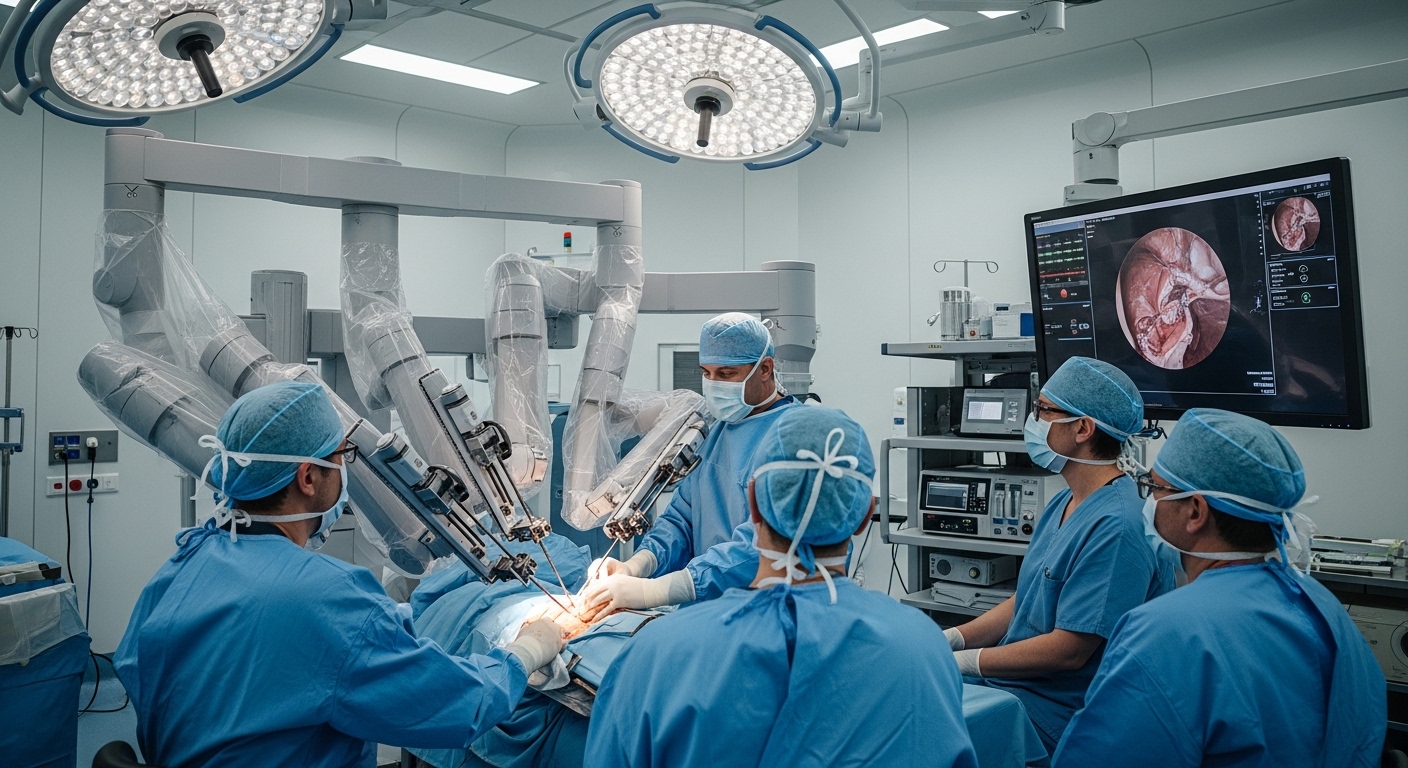
Um die Tragweite der OP-Trends 2026 vollumfänglich zu erfassen, bedarf es zunächst einer klaren Abgrenzung der Begrifflichkeiten, die in der aktuellen Fachdiskussion oft synonym, aber unpräzise verwendet werden. Wenn wir über Robotik KI Chirurgie Trends sprechen, beziehen wir uns auf die Konvergenz zweier technologischer Stränge: der Mechatronik (Robotik) und der Informatik (Künstliche Intelligenz). Die klassische roboterassistierte Chirurgie (RAC) definierte sich primär über die Telemanipulation. Hierbei übersetzt eine Konsole die Handbewegungen des Chirurgen in mikromechanische Bewegungen der Instrumente im Körperinneren des Patienten. Der Vorteil lag bisher in der Skalierung der Bewegung (z.B. 3:1 Übersetzung) und der Filterung des physiologischen Tremors. Doch bis 2026 hat sich die Definition erweitert: Wir sprechen nun von „Intelligent Surgical Systems“.
Diese Systeme zeichnen sich durch minimalinvasive Eingriffe der nächsten Generation aus. Während herkömmliche Laparoskopie starre Instrumente nutzt, bieten moderne Robotiksysteme „Endowrist“-Funktionen mit sieben Freiheitsgraden, die die Beweglichkeit der menschlichen Hand sogar übertreffen. Ein zentraler Begriff hierbei ist die Präzisionsmedizin. Im chirurgischen Kontext bedeutet dies, dass Eingriffe so exakt auf die individuelle Anatomie des Patienten zugeschnitten sind, dass Kollateralschäden an Nerven und Gefäßen minimiert werden. Dies wird durch intraoperative Bildgebung (Augmented Reality) ermöglicht, die über das Sichtfeld des Roboters gelegt wird.
Ein weiteres Schlüsselelement, das bis 2026 zur Marktreife gelangt ist, ist das haptische Feedback. Lange Zeit war das Fehlen des Tastsinns der größte Kritikpunkt an der Robotik. Neue Sensortechnologien ermöglichen es nun, Widerstände, Gewebedichte und Pulsation auf die Konsole des Chirurgen zu übertragen. Dies schließt den sensomotorischen Regelkreis und gibt dem Operateur das Gefühl zurück, das Gewebe direkt zu berühren. Parallel dazu entwickeln sich autonome Assistenzsysteme. Ähnlich wie beim autonomen Fahren (Level 0 bis 5) bewegen wir uns in der Chirurgie auf Level 3 zu: Der Roboter kann unter ständiger Aufsicht des Arztes bestimmte Standardaufgaben (wie das Nähen einer Anastomose oder das Halten der Kamera) selbstständig durchführen. Schließlich ist die Telechirurgie durch den Ausbau von Hochgeschwindigkeitsnetzen keine Nischenanwendung mehr, sondern ein Instrument zur Demokratisierung von Expertenwissen.
Physiologische & Technische Mechanismen (Deep Dive)
Tauchen wir nun tief in die technologischen und physiologischen Mechanismen ein, die diese Revolution ermöglichen. Das Herzstück der modernen OP-Robotik im Jahr 2026 ist nicht mehr nur die Mechanik, sondern die Datenverarbeitung. Die physische Komponente besteht aus hochpräzisen Aktuatoren und Sensoren. Die Arme der neuesten Robotersysteme sind modular aufgebaut und oft „bedside“-montiert, um den Zugang zum Patienten zu erleichtern und Kollisionen zu vermeiden. Die Instrumentenspitzen sind mit mikroskopischen Sensoren ausgestattet, die Dehnungsmessstreifen (Strain Gauges) oder optische Fasern nutzen, um Kräfte im Millinewton-Bereich zu messen. Diese Daten werden in Echtzeit (Latenz unter 5 Millisekunden) an die Steuereinheit gesendet, die daraus haptische Signale für den Chirurgen generiert.
Auf der Seite der Bildgebung nutzen wir stereoskopische 3D-Kameras mit 4K- oder sogar 8K-Auflösung. Doch das reine Bild reicht nicht mehr aus. Hyperspektrale Bildgebung (HSI) und Fluoreszenzangiographie (z.B. mit Indocyaningrün, ICG) sind standardmäßig integriert. Hier kommt die Künstliche Intelligenz ins Spiel, genauer gesagt das Deep Learning und Computer Vision. Convolutional Neural Networks (CNNs) analysieren den Videostream frame-by-frame. Sie segmentieren das Bild in anatomische Strukturen: „Hier ist die Arterie“, „Hier ist der Harnleiter“, „Hier ist Tumorgewebe“. Diese Segmentation erfolgt durch Training an Millionen von OP-Videos. Im Jahr 2026 sind diese Algorithmen so robust, dass sie auch bei Blutungen oder Rauch (durch Kauterisation) zuverlässig funktionieren.
Ein weiterer technischer Mechanismus ist die „Motion Scaling“ und „Tremor Filtration“. Der Algorithmus erkennt den Unterschied zwischen einer willkürlichen Bewegung des Chirurgen und einem unwillkürlichen Zittern (Frequenzbereich ca. 8-12 Hz). Letzteres wird elektronisch herausgefiltert, bevor das Signal an den Roboterarm geht. Bei autonomen Teilaufgaben nutzen die Systeme „Reinforcement Learning“. Ein Roboterarm „lernt“ beispielsweise den optimalen Pfad für eine Nadelstichbewegung, indem er Millionen von Simulationen durchläuft, bevor er am Patienten eingesetzt wird. Die Sicherheit wird hierbei durch sogenannte „Boundary Controls“ gewährleistet. Der Chirurg definiert im virtuellen Raum „No-Fly-Zones“ (z.B. um große Gefäße), in die der Roboterarm mechanisch nicht eindringen kann, selbst wenn der Chirurg die Konsole in diese Richtung steuert. Dies ist die ultimative Verschmelzung von menschlicher Intention und maschineller Sicherheitskontrolle.
Die 5G-Technologie (und erste 6G-Pilotprojekte) spielt für die Telechirurgie eine entscheidende Rolle. Um eine Operation über Distanz durchzuführen, muss die Latenz (Verzögerung) unter 200 Millisekunden bleiben, idealerweise weit darunter. Edge Computing verlagert die Rechenleistung direkt an den Ort des Geschehens (den OP-Saal), während nur die notwendigsten Steuerbefehle über das Netz geschickt werden. Datenkompressionsalgorithmen sorgen dafür, dass das haptische und visuelle Signal synchron bleiben, um die sogenannte „Motion Sickness“ beim Operateur zu verhindern und präzises Arbeiten zu ermöglichen.
Aktuelle Studienlage & Evidenz (Journals)
Die Akzeptanz dieser Technologien im Jahr 2026 basiert nicht auf Marketingversprechen der Hersteller, sondern auf einer breiten, wissenschaftlich fundierten Datenbasis. Die Evidenzlage hat sich in den letzten Jahren massiv verdichtet und zeigt klare Vorteile in spezifischen Indikationen.
Eine umfassende Meta-Analyse, die kürzlich in The Lancet Digital Health veröffentlicht wurde, untersuchte über 50.000 robotisch assistierte Eingriffe im Vergleich zu konventionellen laparoskopischen Verfahren. Die Autoren kamen zu dem Schluss, dass insbesondere bei komplexen onkologischen Eingriffen (wie der Rektumresektion oder Prostatektomie) die Rate an postoperativen Komplikationen signifikant gesenkt werden konnte. Besonders hervorgehoben wurde die Reduktion von Anastomoseninsuffizienzen, was direkt auf die verbesserte Sicht und Präzision der Nahttechnik zurückzuführen ist.
Daten aus dem New England Journal of Medicine (NEJM) belegen den Nutzen von KI-gestützter intraoperativer Diagnostik. In einer vielbeachteten Studie wurde die Genauigkeit von KI-Systemen zur Erkennung von Gallengangsanatomien während der Cholezystektomie evaluiert. Die Studie zeigte, dass die KI-Unterstützung die Rate an Gallengangsverletzungen – eine der gefürchtetsten Komplikationen in der Viszeralchirurgie – um einen statistisch signifikanten Faktor reduzieren konnte, indem sie Chirurgen warnte, bevor kritische Strukturen durchtrennt wurden.
Auch im deutschsprachigen Raum wird intensiv geforscht. Ein Bericht im Deutschen Ärzteblatt analysierte die Lernkurven von Assistenzärzten in der robotischen Chirurgie. Das Ergebnis war überraschend positiv: Durch den Einsatz von hochrealistischen VR-Simulatoren, die auf den Daten realer OPs basieren (Digital Twins), konnte die Zeit bis zur Erreichung der Facharztkompetenz für bestimmte Eingriffe deutlich verkürzt werden. Die Simulation erlaubt das gefahrlose Trainieren von Komplikationsmanagement, was in der Realität am Patienten ethisch nicht vertretbar wäre.
Weitere relevante Studien auf PubMed konzentrieren sich auf die Langzeitergebnisse. Eine Veröffentlichung in JAMA Surgery untersuchte die „Cost-Utility“ (Kosten-Nutzwert-Analyse). Während die Anschaffungskosten für Robotiksysteme und die Instrumentenkosten initial höher sind, zeigte die Studie, dass durch verkürzte Liegezeiten (Length of Stay), geringeren Blutverlust und eine schnellere Rückkehr der Patienten ins Arbeitsleben die gesamtökonomische Bilanz bei hohen Fallzahlen positiv ausfällt. Dies widerlegt das lange gehegte Vorurteil, Robotik sei lediglich ein teures Spielzeug ohne ökonomischen Mehrwert.
Praxis-Anwendung & Implikationen
Was bedeuten diese technologischen und wissenschaftlichen Durchbrüche konkret für den klinischen Alltag, für Ärzte und für Patienten im Jahr 2026? Die Praxis der Chirurgie wandelt sich von einer „One-Man-Show“ zu einem hochgradig interdisziplinären, technologiegestützten Team-Event. Für den Chirurgen verschiebt sich das Anforderungsprofil. Manuelle Dexterität bleibt wichtig, aber die Kompetenz im Umgang mit komplexen Softwaresystemen, die Interpretation von Augmented-Reality-Daten und das Management der Mensch-Maschine-Schnittstelle werden zu Schlüsselqualifikationen. Die Ausbildung muss sich radikal anpassen; das Curriculum 2026 beinhaltet Module zu Medizininformatik und Robotik als Standard.
Für die Krankenhäuser bedeutet dies massive Investitionen in Infrastruktur, aber auch die Chance auf Spezialisierung. Kliniken, die „Smart Operating Rooms“ anbieten, ziehen nicht nur Patienten an, sondern auch Top-Talente unter den Medizinern, die mit der besten Technologie arbeiten wollen. Wir sehen eine Zentralisierung komplexer Eingriffe in High-Volume-Zentren, wo die teuren Roboter effizient ausgelastet werden können. Kleinere Häuser profitieren hingegen durch Telechirurgie-Kooperationen, bei denen Experten aus den Zentren virtuell zugeschaltet werden.
Für den Patienten sind die Implikationen überwiegend positiv, aber auch erklärungsbedürftig. Der Begriff „Minimalinvasive Eingriffe“ bekommt eine neue Dimension: Wir sprechen von „Mikro-Invasivität“. Die Schnitte werden kleiner, das Gewebetrauma geringer, die Schmerzmittelgabe postoperativ reduziert. Dank KI-gestützter präoperativer Planung weiß der Patient oft schon vor dem Eingriff sehr genau, welches Ergebnis zu erwarten ist. Allerdings entsteht auch ein neues Spannungsfeld: Das Vertrauen in die „Maschine“. Das Aufklärungsgespräch 2026 muss beinhalten, welche Schritte autonom oder teilautonom erfolgen und wie die Sicherheitsmechanismen greifen. Patienten müssen verstehen, dass der Roboter kein Ersatz, sondern ein Präzisionswerkzeug in der Hand des erfahrenen Arztes ist.
Ein weiterer Aspekt ist die Datensicherheit. Wenn jeder OP-Schritt in der Cloud analysiert wird, um Algorithmen zu trainieren, ist der Datenschutz von höchster Priorität. Krankenhäuser müssen zu Fort Knox für Gesundheitsdaten werden, um Cyberangriffe auf vernetzte OP-Geräte zu verhindern. Die Praxisanwendung 2026 ist also ein Balanceakt zwischen technologischer Machbarkeit, ökonomischer Effizienz, ethischer Verantwortung und maximaler Patientensicherheit.
Häufige Fragen (FAQ)
In diesem Abschnitt adressieren wir die drängendsten Fragen, die sowohl von medizinischem Fachpersonal als auch von Klinikmanagern und technisch interessierten Patienten an uns herangetragen werden. Die Antworten basieren auf dem technologischen Stand von 2026.
Wie verbessern KI-Algorithmen die operative Präzision?
Künstliche Intelligenz (KI) verbessert die operative Präzision auf mehreren Ebenen, die weit über das menschliche Wahrnehmungsvermögen hinausgehen. Zunächst ermöglicht Computer Vision (CV) eine Echtzeit-Analyse des Operationsfeldes. Algorithmen segmentieren Gewebetypen und können beispielsweise Nervenbahnen oder Blutgefäße, die unter einer Fettschicht verborgen sind, visuell hervorheben (Augmented Reality Overlay). Dies basiert auf der Fusion von präoperativen CT/MRT-Daten mit dem Live-Bild der Endoskop-Kamera. Zweitens kompensiert die KI menschliche Unzulänglichkeiten wie den physiologischen Tremor noch effektiver als rein mechanische Filter, indem sie Bewegungsmuster antizipiert und glättet („Predictive Motion Control“). Drittens ermöglichen KI-gestützte Navigationssysteme eine „No-Fly-Zone“-Funktion: Das System erkennt kritische Strukturen und erhöht den Widerstand an den Bedienelementen oder stoppt die Bewegung komplett, wenn der Chirurg droht, versehentlich gesundes Gewebe zu verletzen. Diese Kombination aus visueller Erweiterung und aktiver Bewegungssteuerung minimiert iatrogene Schäden signifikant.
Welche neuen Robotik-Systeme kommen bis 2026 auf den Markt?
Der Markt für chirurgische Robotik hat sich bis 2026 stark diversifiziert und das Monopol einzelner Anbieter aufgebrochen. Neben den etablierten Multi-Port-Systemen sehen wir einen starken Trend hin zu „Single-Port“-Systemen (SP), bei denen alle Instrumente und die Kamera durch einen einzigen, nur wenige Zentimeter großen Zugang (Trokar) eingeführt werden. Dies reduziert das Trauma der Bauchdecke erheblich. Ein weiterer Trend sind modulare Systeme, bei denen die Roboterarme nicht mehr an einer festen Säule hängen, sondern einzeln am OP-Tisch oder auf mobilen Wagen platziert werden können. Dies erhöht die Flexibilität im oft engen OP-Saal. Zudem drängen Systeme für die Mikrochirurgie (z.B. für Lymphgefäßanastomosen) und die Endoluminale Chirurgie (OPs durch natürliche Körperöffnungen ohne Hautschnitt) auf den Markt. Auch „Soft Robotics“ – flexible, schlangenartige Roboterarme, die sich durch gewundene Anatomien bewegen können – sind 2026 für diagnostische und therapeutische Zwecke in der Pulmonologie und Gastroenterologie verfügbar.
Was zeigen aktuelle Studien zur Sicherheit von OP-Robotern?
Aktuelle Studien, die in renommierten Datenbanken wie PubMed und Cochrane Library gelistet sind, bestätigen ein sehr hohes Sicherheitsniveau moderner Robotiksysteme, das dem der offenen oder konventionell laparoskopischen Chirurgie mindestens ebenbürtig, in vielen Bereichen sogar überlegen ist. Systemausfälle oder technische Defekte während einer OP sind extrem selten (Inzidenz < 0,1%), da redundante Sicherheitssysteme und Notstromaggregate Standard sind. Studien zeigen konsistent, dass die Rate an Konversionen (Notwendigkeit, auf offene Chirurgie umzusteigen) bei robotischen Eingriffen sinkt. Ein kritischer Punkt in der Sicherheitsdiskussion ist die Lernkurve: Daten belegen, dass Komplikationen häufiger in der frühen Phase der Einführung eines Robotikprogramms auftreten. Sobald das Team jedoch etabliert ist und standardisierte Trainings (Simulation) durchlaufen hat, sinkt die Komplikationsrate unter das Niveau konventioneller Verfahren. Die Evidenz deutet darauf hin, dass die Sicherheit primär eine Frage des Trainings und der Team-Kommunikation ist, weniger der Technologie selbst.
Wie verändert sich die Haftung bei KI-gestützten Fehlern?
Die Haftungsfrage ist eines der komplexesten juristischen Themen im Kontext der KI-Chirurgie des Jahres 2026. Grundsätzlich gilt nach wie vor der Grundsatz der „Arzthaftung“: Der operierende Chirurg trägt die letzte Verantwortung für die Entscheidung und die Durchführung des Eingriffs. Solange KI-Systeme als Assistenzsysteme (Decision Support) klassifiziert sind, haftet der Arzt, wenn er einem fehlerhaften Vorschlag der KI folgt, den er hätte als falsch erkennen müssen (Facharztstandard). Mit zunehmender Autonomie (z.B. automatisches Nähen) verschiebt sich die Diskussion jedoch in Richtung der Produkthaftung. Wenn ein autonom agierendes System aufgrund eines Softwarefehlers einen Schaden verursacht, obwohl der Arzt korrekt überwacht hat, rückt der Hersteller in den Fokus. Juristen und Ethikkommissionen arbeiten 2026 an neuen Modellen der „geteilten Verantwortung“ und Versicherungspolicen, die sowohl menschliches Versagen als auch algorithmische Fehler („Black Box Problem“) abdecken. Dokumentation ist hierbei der Schlüssel: „Black Boxes“ im OP zeichnen jede Datenbewegung auf, um im Schadensfall die Kausalkette rekonstruieren zu können.
Warum ist 5G-Technologie entscheidend für die Telechirurgie?
Die 5G-Technologie (und perspektivisch 6G) ist der unverzichtbare „Enabler“ für echte Telechirurgie, da sie drei kritische Anforderungen erfüllt: extrem niedrige Latenz, hohe Bandbreite und hohe Zuverlässigkeit. In der Telechirurgie, wo ein Chirurg an Ort A einen Roboter an Ort B steuert, ist die Zeitverzögerung (Latenz) der kritische Faktor. Ist die Verzögerung zwischen der Handbewegung des Arztes und der visuellen Rückmeldung auf dem Bildschirm zu groß (> 200 ms), wird präzises Operieren unmöglich und gefährlich. 5G reduziert diese Latenz auf unter 10 Millisekunden, was für das menschliche Gehirn als „Echtzeit“ wahrgenommen wird. Zudem ermöglicht die hohe Bandbreite die Übertragung von hochauflösenden 4K/3D-Videostreams und haptischen Datenpaketen ohne Kompressionsverluste. Die Funktion „Network Slicing“ im 5G-Standard erlaubt es zudem, einen Teil des Netzes exklusiv für die medizinische Anwendung zu reservieren, sodass die Verbindung auch dann stabil bleibt, wenn das öffentliche Netz ausgelastet ist. Ohne diese Infrastruktur bliebe Telechirurgie ein experimentelles Wagnis.
Welche Kosten-Nutzen-Analysen gibt es für Robotik im OP?
Die gesundheitsökonomische Bewertung von Robotik im OP hat sich bis 2026 gewandelt. Frühere Analysen kritisierten oft die hohen Anschaffungskosten (CAPEX) von 1-2 Millionen Euro pro System und die hohen laufenden Kosten für Einweginstrumente. Neuere „Cost-Effectiveness“-Analysen betrachten jedoch den gesamten Behandlungspfad („Value-Based Healthcare“). Studien zeigen, dass robotische Chirurgie zwar intraoperativ teurer ist, diese Kosten aber durch signifikante Einsparungen in der postoperativen Phase kompensiert werden können. Dazu gehören: kürzere Verweildauer auf der Intensivstation und im Krankenhaus allgemein, geringere Raten an Wundinfektionen und Re-Operationen sowie ein geringerer Verbrauch von Blutkonserven und Schmerzmitteln. Zudem ermöglichen die ergonomischen Vorteile für Chirurgen ein längeres Berufsleben und weniger krankheitsbedingte Ausfälle im Personal. Bei hoher Auslastung des Systems (hohe Fallzahlen) sinken die Fixkosten pro Fall. Krankenkassen und Kliniken kalkulieren 2026 daher nicht mehr nur die OP-Minute, sondern die „Quality-Adjusted Life Years“ (QALYs) des Patienten und die Gesamtkosten der Episode.
Fazit: Die Symbiose von Mensch und Maschine
Zusammenfassend lässt sich festhalten, dass die OP-Trends für das Jahr 2026 keine bloße Fortsetzung des bisherigen Technologietrends darstellen, sondern einen qualitativen Sprung in der chirurgischen Versorgung markieren. Die Robotik hat ihre Kinderschuhe verlassen und ist, gepaart mit leistungsstarker Künstlicher Intelligenz, zum unverzichtbaren Partner im Operationssaal avanciert. Wir sehen eine Zukunft, in der minimalinvasive Eingriffe noch schonender, noch präziser und noch sicherer werden. Die Integration von haptischem Feedback, autonomen Assistenzfunktionen und Telechirurgie demokratisiert den Zugang zu Spitzenmedizin und gleicht Qualitätsunterschiede zwischen verschiedenen Operateuren und Standorten an.
Doch bei aller technologischen Euphorie bleibt der Faktor Mensch zentral. Der Chirurg des Jahres 2026 ist kein passiver Beobachter, sondern ein hochspezialisierter Manager komplexer Systeme, dessen Empathie, Entscheidungsfähigkeit und klinische Erfahrung durch die Technologie nicht ersetzt, sondern potenziert werden. Die Herausforderungen – seien es ethische Fragen, Datenschutz oder die Finanzierbarkeit – sind real, aber lösbar. Die Studienlage in Journals wie The Lancet, NEJM und dem Deutschen Ärzteblatt liefert die notwendige Evidenz, um diesen Weg mutig weiterzubeschreiten. Für Patienten bedeutet dies: Bessere Ergebnisse, schnellere Heilung und eine Sicherheit, die vor wenigen Jahren noch undenkbar war. Wir stehen am Beginn einer Ära, in der die Grenzen des Machbaren neu definiert werden.
📚 Evidenz & Quellen
Dieser Artikel basiert auf aktuellen Standards. Für Fachinformationen verweisen wir auf:
🧬 Wissenschaftliche Literatur
Vertiefende Recherche in aktuellen Datenbanken:
Dieser Artikel dient ausschließlich der neutralen Information. Er ersetzt keinesfalls die fachliche Beratung durch einen Arzt. Keine Heilversprechen.