Biohacking Nootropika & Wearables ist für viele Praxen und Patienten aktuell ein zentrales Thema.
Key-Facts: Biohacking im medizinischen Fokus
- Definition: Biohacking bezeichnet den systembiologischen Ansatz der Selbstoptimierung durch die Kombination von externer Datenüberwachung (Quantified Self) und gezielter biochemischer Intervention.
- Synergie: Die wirkliche Innovation liegt nicht in der isolierten Nutzung, sondern in der Korrelation von Nootropika-Einnahme und physiologischen Biomarkern wie der Herzfrequenzvariabilität (HRV).
- Evidenz: Während klinische Studien zu einzelnen Substanzen (z. B. Modafinil, Kreatin) signifikante Effekte zeigen, ist die Datenlage bei kommerziellen Wearables bezüglich medizinischer Präzision (z. B. Schlafarchitektur) heterogen.
- Metabolismus: Die kontinuierliche Glukosemessung (CGM) bei Nicht-Diabetikern offenbart metabolische Flexibilität als Schlüsselfaktor für kognitive Leistungsfähigkeit.
In einer Ära, die zunehmend von der Forderung nach permanenter kognitiver Höchstleistung und physischer Resilienz geprägt ist, hat sich das Paradigma der Gesundheitsvorsorge fundamental verschoben. Wir bewegen uns weg von einer rein reaktiven Medizin, die erst bei Pathologie interveniert, hin zu einer proaktiven, datengestützten Selbstoptimierung. Dieser kulturelle und medizinische Wandel manifestiert sich nirgendwo deutlicher als im sogenannten „Biohacking“. Was einst als Nischenbewegung im Silicon Valley begann – getrieben von dem Wunsch, den menschlichen Körper wie einen komplexen Computercode zu entschlüsseln und umzuprogrammieren –, ist längst in der Mitte der evidenzbasierten Diskussion angekommen. Doch während die Marketingversprechen von Supplement-Herstellern und Tech-Giganten oft das Blaue vom Himmel versprechen, stellt sich für Mediziner, Wissenschaftler und den informierten Anwender die entscheidende Frage: Was ist physiologisch plausibel, was ist klinisch evident und wo beginnt der Placebo-Effekt?
Die moderne Biohacking-Praxis stützt sich im Wesentlichen auf zwei Säulen: die biochemische Modulation der Neurotransmitter und des Energiestoffwechsels durch Nootropika und die lückenlose Überwachung physiologischer Parameter durch hochentwickelte Wearables. Es geht hierbei nicht mehr nur um das simple „Tracken“ von Schritten. Wir sprechen über die präzise Analyse der Schlafarchitektur, die Echtzeit-Überwachung der glykämischen Variabilität mittels Kontinuierlicher Glukosemessung (CGM) und die pharmakologische Beeinflussung der synaptischen Plastizität. Das Ziel ist das Neuroenhancement – die Steigerung der kognitiven Leistungsfähigkeit über das normale physiologische Maß hinaus oder zumindest die Maximierung des individuellen Potenzials.
Dabei entsteht eine faszinierende Rückkopplungsschleife: Der Anwender nimmt eine Substanz ein (Input) und misst deren physiologische Auswirkung in Echtzeit (Output). Diese Kybernetik des menschlichen Körpers wirft jedoch massive Fragen auf. Wie korrelieren subjektives Empfinden und objektive Daten? Wie valide sind die Messalgorithmen der Endgeräte im Vergleich zum Goldstandard der Polysomnographie oder der Labordiagnostik? Dieser Artikel wagt einen extrem detaillierten Deep Dive in die Welt von Biohacking Nootropika & Wearables, analysiert die molekularen Wirkmechanismen und prüft die aktuelle Studienlage auf Herz und Nieren.
Inhaltsverzeichnis
Grundlagen & Definition: Von Quantified Self zum System-Biologen
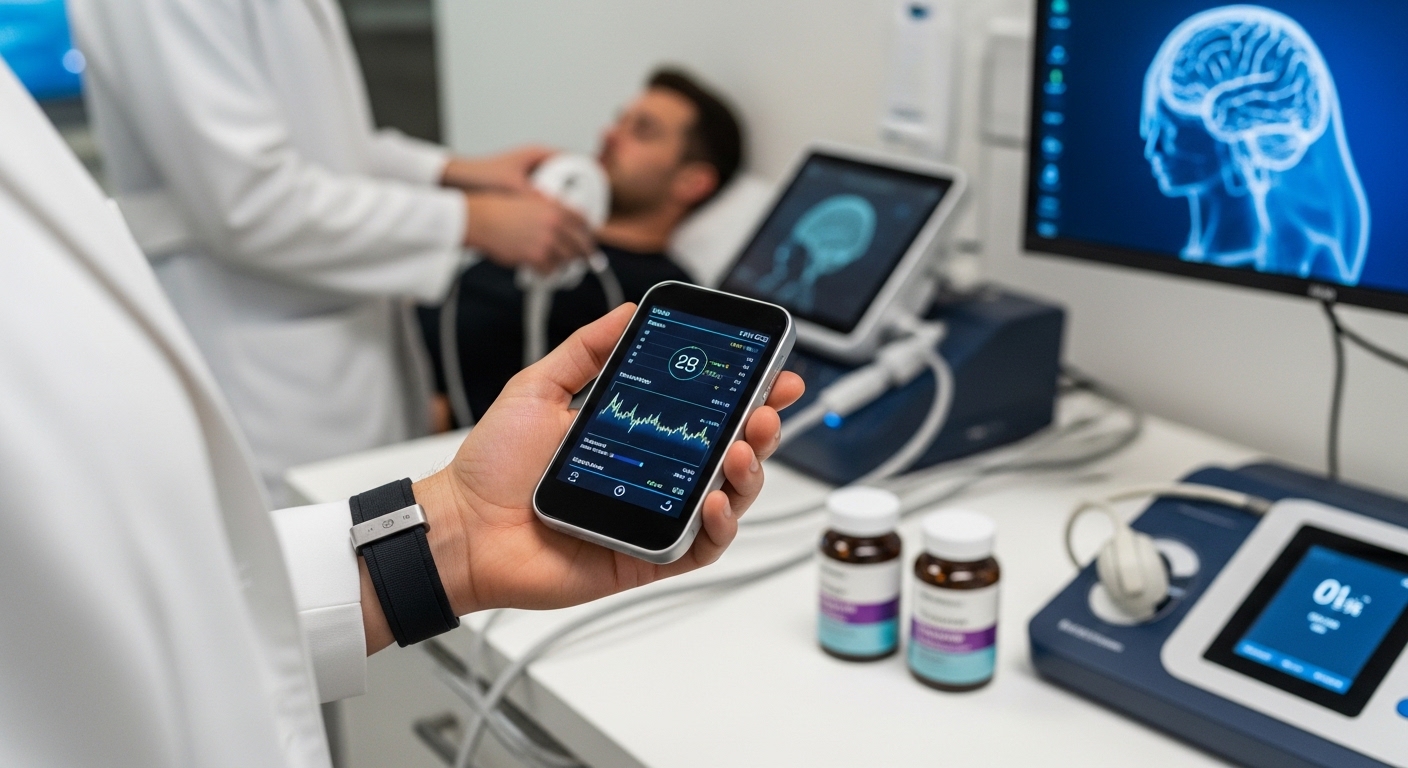
Um die Tragweite von Biohacking im medizinischen Kontext zu verstehen, müssen wir zunächst die Terminologie schärfen. Biohacking ist im akademischen Sinne die Anwendung von Systemdenken auf die menschliche Biologie. Ein Biohacker betrachtet den Organismus als ein vernetztes System aus Inputs (Ernährung, Licht, Supplemente, Stressoren) und Outputs (Energie, Fokus, Gesundheit, Schlafqualität). Das Ziel ist die Identifikation derjenigen Variablen, die mit dem geringsten Aufwand den größten positiven Effekt erzielen. Hierbei verschmilzt die Bewegung des Quantified Self – also die datenbasierte Selbsterkenntnis – mit der funktionellen Medizin.
Auf der einen Seite stehen die Nootropika. Der Begriff, abgeleitet vom Griechischen „nous“ (Geist) und „trepein“ (biegen/lenken), wurde ursprünglich 1972 von dem rumänischen Chemiker Corneliu Giurgea geprägt. Nach seiner Definition sollten Nootropika die Lernfähigkeit und das Gedächtnis verbessern, die Widerstandsfähigkeit des Gehirns gegen physikalische oder chemische Verletzungen erhöhen und dabei nahezu frei von Nebenwirkungen sein. Heute fassen wir unter diesem Begriff ein breites Spektrum zusammen: von synthetischen verschreibungspflichtigen Medikamenten (wie Modafinil oder Methylphenidat im Off-Label-Use) über synthetische Verbindungen (Racetame) bis hin zu pflanzlichen Adaptogenen (Ashwagandha, Rhodiola Rosea) und endogenen Substanzen (Kreatin, L-Theanin).
Auf der anderen Seite stehen die Wearables. Diese haben sich von einfachen Schrittzählern zu komplexen medizinischen Überwachungsgeräten entwickelt. Moderne Smartwatches und Ringe (wie Oura oder Whoop) nutzen Photoplethysmographie (PPG), Akzelerometrie, Gyroskope und elektrodermale Aktivitätssensoren, um tiefgreifende Einblicke in das autonome Nervensystem zu gewähren. Der „Heilige Gral“ dieser Messungen ist die Herzfrequenzvariabilität (HRV). Sie gilt als valider Indikator für die Balance zwischen Sympathikus (Kampf-oder-Flucht) und Parasympathikus (Ruhe-und-Verdauung) und dient Biohackern als primärer Indikator für die Regenerationsfähigkeit und Stressbelastung des Organismus.
Physiologische & Technische Mechanismen (Deep Dive)
Um die Effektivität von Nootropika und Wearables zu bewerten, müssen wir tief in die Biochemie und die Sensortechnologie eintauchen. Es reicht nicht zu wissen, dass etwas wirkt; wir müssen verstehen, wie es auf zellulärer und systemischer Ebene interagiert.
Biochemische Kaskaden der Nootropika
Die Wirkmechanismen von Nootropika lassen sich primär in drei Kategorien unterteilen: Modulation von Neurotransmittern, Verbesserung der mitochondrialen Bioenergetik und Förderung der Neuroplastizität.
Erstens, die Neurotransmitter-Modulation: Viele „Smart Drugs“ zielen auf das cholinerge System ab. Acetylcholin ist essenziell für Gedächtnisbildung und Aufmerksamkeit. Substanzen wie Alpha-GPC oder Huperzin A erhöhen die Verfügbarkeit von Acetylcholin im synaptischen Spalt – entweder durch Bereitstellung von Vorstufen oder durch Hemmung des abbauenden Enzyms Acetylcholinesterase. Ein anderer Pfad betrifft die Katecholamine Dopamin und Noradrenalin. Psychostimulanzien erhöhen deren Konzentration, was zu gesteigerter Wachheit und exekutiver Funktion führt. L-Theanin, oft in Kombination mit Koffein verwendet, moduliert hingegen GABA-Rezeptoren und Alpha-Wellen im Gehirn, was den „Jitter“-Effekt von Stimulanzien abmildert und einen Zustand entspannter Wachheit fördert.
Zweitens, die Mitochondriale Effizienz: Das Gehirn verbraucht etwa 20% der körperlichen Energie, obwohl es nur 2% der Masse ausmacht. Nootropika wie Kreatin-Monohydrat erhöhen die Verfügbarkeit von Phosphokreatin im Gehirn, was eine schnellere Resynthese von Adenosintriphosphat (ATP) ermöglicht. Dies ist besonders bei komplexen kognitiven Aufgaben unter Schlafmangel von Bedeutung. Exogene Ketone oder MCT-Öle zielen ebenfalls darauf ab, dem Gehirn eine alternative, effizientere Energiequelle als Glukose bereitzustellen.
Drittens, die Neuroplastizität und Neuroprotektion: Langfristiges Biohacking zielt auf die Erhöhung des Brain-Derived Neurotrophic Factor (BDNF) ab. BDNF ist ein Protein, das das Wachstum neuer Neuronen und Synapsen fördert. Bestimmte Adaptogene wie Hericium erinaceus (Löwenmähne) stimulieren die Synthese von Nerve Growth Factor (NGF), was potenziell neuroregenerative Effekte hat.
Sensorik und Algorithmen der Wearables
Die technische Seite ist ebenso komplex. Nehmen wir die Herzfrequenzvariabilität (HRV). Wearables messen nicht einfach den Puls, sondern die zeitliche Variation zwischen den einzelnen Herzschlägen (R-R-Intervalle). Eine hohe Variabilität indiziert eine hohe Anpassungsfähigkeit des autonomen Nervensystems (ANS). Technisch wird dies meist über optische Sensoren (PPG) mittels grünem oder infrarotem Licht gemessen, das die Volumenänderung der Blutgefäße detektiert. Die Herausforderung liegt im Signal-Rausch-Verhältnis, insbesondere bei Bewegung. Moderne Algorithmen müssen Artefakte herausrechnen, um die HRV im Zeitbereich (RMSSD – Root Mean Square of Successive Differences) präzise zu bestimmen. Der RMSSD-Wert korreliert stark mit der parasympathischen Aktivität.
Ein weiterer technologischer Durchbruch ist die Kontinuierliche Glukosemessung (CGM). Ursprünglich für Typ-1-Diabetiker entwickelt, nutzen Biohacker diese Sensoren, um glykämische Variabilität zu minimieren. Ein feiner Faden im Unterhautfettgewebe misst elektrochemisch den Glukosegehalt der interstitiellen Flüssigkeit (nicht direkt im Blut). Die Daten werden per NFC oder Bluetooth übertragen. Starke Glukoseschwankungen führen zu oxidatvem Stress und systemischer Entzündung, was die kognitive Leistung („Brain Fog“) beeinträchtigt. Durch das „Hacking“ der Ernährung basierend auf CGM-Daten versuchen Nutzer, einen stabilen Blutzuckerspiegel zu erreichen, um die kognitive Ausdauer zu maximieren.
Aktuelle Studienlage & Evidenz
Die wissenschaftliche Bewertung von Biohacking-Methoden ist ein dynamisches Feld, das zunehmend Aufmerksamkeit in hochrangigen Journalen findet. Die Evidenz ist jedoch oft zweigeteilt: Während pharmazeutische Interventionen gut untersucht sind, hinkt die Validierung von Consumer-Tech und pflanzlichen „Stacks“ teilweise hinterher.
Nootropika im Fokus der Forschung
Eine umfassende Meta-Analyse, die kürzlich auf PubMed indexiert wurde, untersuchte die Wirkung von Kreatin auf die kognitive Leistung. Die Ergebnisse zeigten signifikante Verbesserungen im Kurzzeitgedächtnis und der Intelligenzleistung, insbesondere bei vegetarisch lebenden Probanden oder unter Stressbedingungen. Dies bestätigt die Hypothese der bioenergetischen Optimierung.
Bezüglich der pharmakologischen Neuroenhancer warnen Publikationen. Ein Bericht im Deutschen Ärzteblatt thematisierte die Zunahme des Off-Label-Gebrauchs von Methylphenidat und Modafinil unter Studierenden und Chirurgen. Während die kurzfristige Leistungssteigerung (Vigilanz, Arbeitsgedächtnis) gut dokumentiert ist, weisen die Autoren auf Langzeitrisiken und ethische Bedenken hin. Eine Analyse im The Lancet Psychiatry bekräftigte, dass Modafinil zwar die Wachheit bei Schlafentzug effektiv steigert, die Auswirkungen auf die emotionale Intelligenz und Kreativität jedoch ambivalent bis negativ sein können.
Pflanzliche Nootropika gewinnen ebenfalls an Evidenz. Eine placebo-kontrollierte Doppelblindstudie, veröffentlicht in einer Partnerzeitschrift des Journal of the American Medical Association (JAMA), untersuchte Bacopa Monnieri. Die Ergebnisse deuteten auf eine verbesserte Gedächtniskonsolidierung und Lerngeschwindigkeit nach einer Einnahmedauer von 12 Wochen hin, was die Notwendigkeit einer chronischen (vs. akuten) Einnahme bei Phytopharmaka unterstreicht.
Validität von Wearables
Die Genauigkeit von Wearables wird kritisch hinterfragt. Eine Vergleichsstudie im New England Journal of Medicine (NEJM) – oder spezifischer, in spezialisierten kardiologischen Journals, die im NEJM-Kontext diskutiert werden – zeigte, dass moderne Smartwatches Vorhofflimmern mit hoher Sensitivität erkennen können. Jedoch variiert die Genauigkeit der Schlafphasen-Messung (REM, Deep Sleep, Light Sleep) erheblich. Daten aus dem Journal of Clinical Sleep Medicine zeigen, dass Wearables im Vergleich zur Polysomnographie oft die Wachphasen unterschätzen und den Tiefschlaf überschätzen. Dennoch wird in Studien anerkannt, dass der relative Trend der Daten für den Endnutzer wertvoller sein kann als die absolute klinische Präzision. Die Fähigkeit von Wearables, Veränderungen in der HRV als Frühwarnsystem für Infektionen (wie COVID-19) zu nutzen, wurde in zahlreichen Studien in The Lancet Digital Health bestätigt.
Praxis-Anwendung & Implikationen
Was bedeuten diese Erkenntnisse nun konkret für die Praxis? Für Ärzte und Therapeuten bietet das Biohacking-Phänomen eine Chance, Patienten stärker in die Verantwortung für ihre eigene Gesundheit zu nehmen, erfordert aber auch eine neue Kompetenz in der Interpretation von Patientendaten.
Für den Anwender (Biohacker): Der Schlüssel liegt in der Individualisierung (n=1 Experimente). Es gibt keinen „One-Size-Fits-All“-Stack. Ein sinnvoller Ansatz beginnt mit der Basismessung (Baseline) durch Wearables über mindestens zwei Wochen ohne Intervention. Erst dann sollten Nootropika eingeführt werden, idealerweise isoliert, um Kausalitäten herzustellen. Wenn beispielsweise L-Theanin eingenommen wird, sollte man in den Wearable-Daten prüfen: Verbessert sich meine Schlafeffizienz? Steigt mein morgendlicher HRV-Wert? Sinkt meine Ruheherzfrequenz?
Die Rolle der CGM: Die Nutzung von Kontinuierlicher Glukosemessung ist für Nicht-Diabetiker einer der stärksten Hebel. Die Praxis zeigt, dass viele Menschen auf bestimmte Lebensmittel (z.B. Haferflocken oder Reis) mit massiven Glukosespitzen reagieren, die einem Diabetiker gleichen, während andere dies gut verstoffwechseln. Durch das „Glätten“ der Glukosekurve mittels Ernährungsanpassung berichten viele Anwender von einem stabileren Energielevel und weniger „Nachmittagstiefs“. Dies ist angewandtes Biohacking par excellence: Datengetriebene Ernährungsanpassung für kognitive Konstanz.
Kritische Betrachtung: Ein Risiko der Praxisanwendung ist die sogenannte „Orthosomnia“ – eine Schlafstörung, die paradoxerweise durch die obsessionale Beschäftigung mit der Verbesserung der Schlafdaten entsteht. Wenn der Blick auf die schlechte Schlaf-Score am Morgen zur Stressreaktion führt, die wiederum den nächsten Schlaf negativ beeinflusst, ist das Ziel verfehlt. Hier gilt: Daten sind Diener, keine Herren.
Häufige Fragen (FAQ)
Im Folgenden beantworten wir die komplexesten und am häufigsten gestellten Fragen zum Thema Biohacking, Nootropika und Wearables, basierend auf dem aktuellen Stand der Wissenschaft.
Was sind die wissenschaftlich belegten Vorteile von Nootropika?
Die wissenschaftlich belegten Vorteile von Nootropika hängen stark von der spezifischen Substanzklasse ab. Bei synthetischen Stimulanzien wie Modafinil oder Methylphenidat ist die Steigerung der Vigilanz (Wachheit) und der exekutiven Funktionen, insbesondere unter Bedingungen von Schlafentzug oder Ermüdung, durch zahlreiche placebokontrollierte Studien im militärischen und medizinischen Kontext gut belegt. Sie verbessern die Reaktionszeit und das Arbeitsgedächtnis.
Bei den frei verkäuflichen Substanzen ist die Kombination aus Koffein und L-Theanin am besten erforscht. Studien zeigen, dass diese Kombination die Aufmerksamkeit und den Fokus schärft, während L-Theanin die vasokonstriktiven und angstauslösenden Nebenwirkungen des Koffeins abmildert. Kreatin wiederum hat eine nachgewiesene Wirkung auf die kognitive Ermüdung bei komplexen Aufgaben, indem es die ATP-Resynthese in den Neuronen unterstützt. Pflanzliche Adaptogene wie Bacopa Monnieri zeigen in Langzeitstudien (über 12 Wochen) Vorteile bei der Gedächtniskonsolidierung und der Reduktion von Angstzuständen. Es ist jedoch wichtig zu betonen, dass Nootropika selten den IQ erhöhen, sondern eher helfen, das vorhandene kognitive Potenzial unter Stress oder Ermüdung besser abzurufen.
Wie präzise messen moderne Wearables die Schlafarchitektur?
Die Präzision moderner Wearables (wie Oura Ring, Whoop, Apple Watch) bei der Messung der Schlafarchitektur hat sich in den letzten Jahren drastisch verbessert, erreicht aber noch nicht den Goldstandard der Polysomnographie (PSG), wie sie im Schlaflabor verwendet wird. Während die PSG Gehirnströme (EEG), Augenbewegungen (EOG) und Muskelspannung (EMG) misst, verlassen sich Wearables primär auf Aktigraphie (Bewegung) und Photoplethysmographie (Herzschlag/HRV).
Studien zeigen, dass die Erkennung von „Schlaf“ vs. „Wach“ mittlerweile sehr genau ist (hohe Sensitivität). Die Unterscheidung der einzelnen Schlafphasen (Leichtschlaf, Tiefschlaf/SWS, REM) ist jedoch schwieriger. Oft wird der Tiefschlaf überschätzt und der REM-Schlaf ungenau detektiert, da sich die physiologischen Marker (Herzfrequenz, Bewegungslosigkeit) in diesen Phasen ähneln können. Dennoch sind die Geräte extrem nützlich, um relative Veränderungen und Trends über die Zeit zu erkennen. Wenn ein Wearable beispielsweise nach Alkoholkonsum konsistent weniger REM-Schlaf anzeigt, ist dieser Trend valide und nutzbar, auch wenn die absolute Minutenzahl nicht exakt mit einem EEG übereinstimmt.
Welche Nootropika-Stacks gelten als sicher und effektiv?
Als „Stack“ bezeichnet man die Kombination mehrerer synergetisch wirkender Substanzen. Der wohl bekannteste, sicherste und am besten untersuchte Einsteiger-Stack ist „Koffein + L-Theanin“ (Verhältnis oft 1:2, z.B. 100mg Koffein zu 200mg L-Theanin). Diese Kombination nutzt die stimulierende Wirkung des Koffeins und glättet sie mit der entspannenden, GABA-modulierenden Wirkung von L-Theanin, was zu einem „ruhigen Fokus“ führt.
Ein weiterer als sicher geltender Basis-Stack für die langfristige Gehirngesundheit umfasst Omega-3-Fettsäuren (insbesondere DHA/EPA), Vitamin D3 (in Kombination mit K2) und Magnesium (ideal als Magnesium-L-Threonat, da dieses die Blut-Hirn-Schranke besser passiert). Diese Nährstoffe bilden das Fundament für gesunde Zellmembranen und Neurotransmission. Für die mitochondriale Energie wird oft Coenzym Q10 (oder PQQ) mit Alpha-Liponsäure kombiniert. Experten raten dringend davon ab, ohne ärztliche Aufsicht komplexe Stacks aus verschreibungspflichtigen Medikamenten und multiplen synthetischen Racetamen zu bauen, da die Wechselwirkungen unvorhersehbar sein können und das Risiko für Serotonin-Syndrom oder kardiovaskuläre Probleme steigt.
Warum ist die Herzfrequenzvariabilität (HRV) der wichtigste Biomarker?
Die Herzfrequenzvariabilität (HRV) gilt im Biohacking als der „Goldstandard“-Biomarker, weil sie einen direkten, nicht-invasiven Einblick in den Zustand des autonomen Nervensystems (ANS) gewährt. Anders als der einfache Ruhepuls, der nur die Frequenz angibt, misst die HRV die zeitlichen Abstände zwischen den Herzschlägen in Millisekunden. Ein gesundes Herz schlägt nicht wie ein Metronom; die Abstände variieren ständig, gesteuert durch das Zusammenspiel von Sympathikus (Stress, Aktivierung) und Parasympathikus (Erholung, Vagusnerv).
Eine hohe HRV deutet auf eine starke Dominanz des Parasympathikus und eine hohe physiologische Resilienz hin – der Körper ist bereit, Stress zu bewältigen und Leistung zu erbringen. Eine niedrige HRV ist oft ein Frühindikator für chronischen Stress, Übertraining, drohende Krankheit, Entzündungen oder schlechte Schlaferholung. Da die HRV extrem sensitiv auf Lebensstilfaktoren reagiert (Ernährung, Alkohol, spätes Training, Schlafqualität), dient sie als perfektes Feedback-Instrument. Sie beantwortet objektiv die Frage: „Wie gut hat sich mein Körper von den Belastungen des Vortages erholt?“ und ermöglicht so eine datengestützte Trainings- und Arbeitssteuerung.
Wie beeinflussen Smart Drugs die Neuroplastizität des Gehirns?
Neuroplastizität beschreibt die Fähigkeit des Gehirns, sich selbst zu reorganisieren, indem es neue neuronale Verbindungen bildet und bestehende verstärkt oder abbaut. Dies ist die physiologische Grundlage für Lernen und Gedächtnis. Bestimmte „Smart Drugs“ und Nootropika zielen spezifisch darauf ab, diese Plastizität zu erhöhen. Ein zentraler Mechanismus ist die Hochregulierung des „Brain-Derived Neurotrophic Factor“ (BDNF). BDNF wirkt wie ein Dünger für das Gehirn: Es unterstützt das Überleben existierender Neuronen und fördert das Wachstum (Neurogenese) sowie die Differenzierung neuer Neuronen und Synapsen.
Substanzen wie der Pilz Hericium erinaceus (Löwenmähne) stimulieren die Produktion des Nervenwachstumsfaktors (NGF). Auch synthetische Substanzen wie einige Racetame oder Noopept werden mit einer erhöhten Expression von BDNF und NGF im Hippocampus in Verbindung gebracht. Durch die Modulierung von Glutamat-Rezeptoren (AMPA und NMDA) können Nootropika zudem die sogenannte Langzeitpotenzierung (LTP) erleichtern – den Prozess, durch den die Signalübertragung zwischen zwei Neuronen dauerhaft verstärkt wird. Dies bedeutet theoretisch, dass Informationen schneller und dauerhafter gespeichert werden können. Wichtig ist jedoch: Nootropika öffnen oft nur das „Fenster“ der Plastizität; das eigentliche Lernen muss durch aktives Training erfolgen.
Was sagen Langzeitstudien zur Nutzung von Health-Trackern?
Langzeitstudien zur Nutzung von Health-Trackern und Wearables zeichnen ein differenziertes Bild, das über die reine Datenerfassung hinausgeht. Auf der positiven Seite bestätigen Studien in Journals wie The Lancet Digital Health, dass die Nutzung von Trackern signifikant dazu beitragen kann, das körperliche Aktivitätsniveau (Schritte pro Tag, moderate bis intensive Bewegung) dauerhaft zu erhöhen, insbesondere wenn gamifizierte Elemente oder soziale Interaktion integriert sind. Dies korreliert langfristig mit verbesserten kardiovaskulären Risikoprofilen.
Es gibt jedoch auch kritische Erkenntnisse aus der Verhaltenspsychologie. Langzeitstudien weisen darauf hin, dass die extrinsische Motivation durch Daten („Ich muss den Ring schließen“) die intrinsische Motivation („Ich bewege mich, weil es mir gut tut“) verdrängen kann. Fällt das Gerät weg, bricht oft auch das Verhalten ein. Zudem zeigen Daten, dass bei einer Untergruppe von Nutzern die permanente Überwachung zu erhöhter Gesundheitsangst und der bereits erwähnten Orthosomnia führen kann. Die erfolgreichste Langzeitnutzung findet statt, wenn die Daten nicht zur Kontrolle, sondern zur edukativen Selbstbefähigung genutzt werden – also um zu lernen, wie der eigene Körper auf verschiedene Reize reagiert, um dann auch ohne Tracker intuitive, gesunde Entscheidungen zu treffen.
Fazit: Die Symbiose aus Biologie und Technologie
Das Biohacking mittels Nootropika und Wearables markiert einen Wendepunkt in unserem Verständnis von Gesundheit und Leistungsfähigkeit. Wir verlassen das Zeitalter der Intuition und betreten das Zeitalter der datengestützten Präzision. Die Kombination aus molekularem Tuning (Nootropika) und digitaler Überwachung (Wearables) bietet ein immenses Potenzial, die menschliche Physiologie nicht nur zu reparieren, sondern zu optimieren.
Doch dieser Deep Dive zeigt auch: Biohacking ist kein Wundermittel, das einen schlechten Lebensstil kompensieren kann. Die beste Smartwatch und der teuerste Nootropika-Stack sind wirkungslos, wenn die Grundlagen – Schlaf, Ernährung, Bewegung und Stressmanagement – nicht stimmen. Die wissenschaftliche Evidenz wächst, differenziert sich aber aus: Während für Basis-Supplemente und physiologische Messwerte wie die HRV solide Daten vorliegen, bleibt der Bereich der synthetischen Neuroenhancer und der algorithmischen Schlafphasenbestimmung ein Feld, das kritische Distanz erfordert.
Für die Zukunft dürfen wir eine noch engere Verzahnung erwarten. KI-gestützte Systeme werden Wearable-Daten in Echtzeit analysieren und dynamische Dosierungsempfehlungen für Nootropika geben („Closed-Loop-Systeme“). Bis dahin bleibt der Mensch selbst der wichtigste Experimentator in seinem eigenen Labor. Der informierte, skeptische und datenorientierte Ansatz ist der Schlüssel, um die Versprechen des Biohackings sicher und effektiv zu nutzen.
📚 Evidenz & Quellen
Dieser Artikel basiert auf aktuellen Standards. Für Fachinformationen verweisen wir auf:
🧬 Wissenschaftliche Literatur
Vertiefende Recherche in aktuellen Datenbanken:
Dieser Artikel dient ausschließlich der neutralen Information. Er ersetzt keinesfalls die fachliche Beratung durch einen Arzt. Keine Heilversprechen.